Общие сведения
Анемия у детей (малокровие) – патологическое состояние, сопровождающееся снижением уровня гемоглобина и эритроцитов в крови ребенка. Анемия у детей – чрезвычайно распространенное заболевание в современной педиатрии. Около 40% случаев анемии диагностируется у детей в возрасте до 3-х лет; 30% — в пубертатном периоде; остальные – в различные возрастные периоды развития ребенка.

В12-дефицитная анемия — симптомы и лечение
Что такое в12-дефицитная анемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Слесарчук Ольги Александровны, гематолога со стажем в 16 лет.

Гематолог, стаж 16 лет
Над статьей доктора
Слесарчук Ольги Александровны
работали
литературный редактор
Юлия Липовская,
научный редактор
Всеволод Потапенко
и
шеф-редактор
Маргарита Тихонова
Дата публикации 9 марта 2021
Обновлено 26 апреля 2021
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Симптомы анемии у детей
Норма гемоглобина крови у детей до 6 лет составляет 125–135 г/л; об анемии у ребенка говорят в том случае, если этот показатель опускается ниже 110 г/л (у детей до 5 лет) и ниже 120 г/л (у детей старше 5 лет).
Видимые изменения при анемии у детей наблюдаются со стороны кожи и ее придатков: кожные покровы становятся бледными, сухими, шелушащимися; ногти деформируются и становятся ломкими; волосы теряют здоровый блеск. Характерным признаком анемии у детей является симптом Филатова – бледность мочек ушей при осмотре в проходящем свете. При тяжелых формах анемии у детей появляются трещины на ладонях и подошвах, в уголках рта; развивается афтозный стоматит, глоссит. Дети с анемией ослаблены, астеничны, часто болеют ОРВИ, бронхитами и пневмониями, острыми кишечными инфекциями.
Со стороны нервной системы, испытывающей гипоксию, отмечается вялость, плаксивость, быстрая истощаемость, головокружения, поверхностный сон, энурез. Выявляется снижение мышечного тонуса, ребенок плохо переносит физические нагрузки, быстро утомляется. У детей первого года жизни отмечается гипотрофия, происходит регресс психомоторного развития.
При анемии у детей выявляются нарушения функции сердечно-сосудистой системы в виде артериальной гипотонии, ортостатических коллапсов, обмороков, тахикардии, систолического шума. Со стороны пищеварительной системы у детей с анемией наблюдаются частые срыгивания и рвота после кормления, метеоризм, диарея или запоры, пониженный аппетит, возможно увеличение селезенки и печени.
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др. Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр. Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.

Изменения ногтей при железодефицитной анемии
Железодефицитная анемия у детей – разновидность дефицитной анемии, в основе которой лежит абсолютная или относительная недостаточность железа в организме. Распространенность железодефицитной анемии среди детей первых 3-х лет жизни составляет 40%; среди подростков – 30%; среди женщин репродуктивного возраста — 44%. Без преувеличения можно констатировать, что железодефицитная анемия является наиболее частой формой, с которой приходится сталкиваться специалистам в области педиатрии, акушерства и гинекологии, терапии, гематологии.
Во время внутриутробного развития железо поступает в организм ребенка от матери через плаценту. Наиболее усиленный трансплацентарный транспорт железа происходит в период с 28 по 32-ю недели беременности. К моменту рождения организм доношенного ребенка содержит 300-400 мг железа, недоношенного – только 100-200 мг. У новорожденного расход неонатального железа происходит на синтез Hb, ферментов, миоглобина, регенерацию кожи и слизистых оболочек, компенсацию физиологических потерь с потом, мочой, калом и т. Быстрые темпы роста и развития детей раннего возраста обусловливают повышенную потребность организма в железе. Между тем, усиленное расходование железа из депо приводит к быстрому истощению его резервов: у доношенных детей к 5–6-му месяцу жизни, у недоношенных — к 3-му месяцу.
Для нормального развития суточный рацион новорожденного должен содержать 1,5 мг железа, а рацион ребенка 1–3 лет — не менее 10 мг. Если потери и расходование железа преобладают над его поступлением и усвоением, у ребенка развивается железодефицитная анемия. Недостаток железа и железодефицитная анемия у детей способствует гипоксии органов и тканей, снижению иммунитета, росту инфекционной заболеваемости, нарушению нервно-психического развития ребенка.
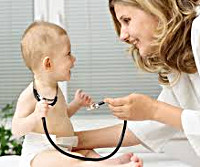
Симптомы ЖДА у детей
Клиника железодефицитной анемии у ребенка неспецифична и может протекать с преобладанием астено-вегетативного, эпителиального, диспепсического, сердечно-сосудистого, иммунодефицитного, гепатолиенального синдрома.
Астено-вегетативные проявления у детей с железодефицитной анемией обусловлены гипоксией органов и тканей, в т. головного мозга. При этом может отмечаться мышечная гипотония, отставание ребенка в физическом и психомоторном развитии (в тяжелых случаях – интеллектуальная недостаточность), плаксивость, раздражительность, вегето-сосудистая дистония, головокружения, ортостатические коллапсы, обмороки, энурез.
Эпителиальный синдром при железодефицитной анемии у детей сопровождается изменениями со стороны кожи и ее придатков: сухостью кожных покровов, гиперкератозом кожи локтей и коленей, появлением трещин на слизистой рта (ангулярный стоматит), глосситом, хейлитом, тусклостью и активным выпадением волос, ломкостью и исчерченностью ногтей.
Диспепсические явления при железодефицитной анемии у детей включают снижение аппетита, анорексию, дисфагию, запоры, метеоризм, диарею. Характерно изменение обоняния (пристрастие к резким запахам бензина, лаков, красок) и вкуса (желание есть мел, землю и пр. Поражение ЖКТ приводит к нарушению процесса всасывания железа, что еще более утяжеляет железодефицитную анемию у детей.
Изменения со стороны сердечно-сосудистой системы возникают при тяжелой степени железодефицитной анемии у детей и характеризуются тахикардией, одышкой, артериальной гипотонией, сердечными шумами, дистрофией миокарда. Синдром иммунодефицита характеризуется длительным немотивированным субфебрилитетом, частыми ОКИ и ОРВИ, тяжелым и затяжным течением инфекций.
Гепатолиенальный синдром (гепатоспленомегалия) обычно встречается у детей, страдающих тяжелой железодефицитной анемией, рахитом и анемией.
Причины
В развитии железодефицитной анемии у детей могут быть задействованы антенатальные и постнатальные факторы.
К антенатальным факторам относится несформированность депо железа во внутриутробном периоде. В этом случае железодефицитная анемия обычно развивается у детей в возрасте до 1,5 лет. Раннему развитию анемии у ребенка могут способствовать токсикозы, анемия беременной, инфекционные заболевания женщины в период гестации, угроза прерывания беременности, фетоплацентарная недостаточность, отслойка плаценты, многоплодная беременность, преждевременная или поздняя перевязка пуповины у ребенка. Наиболее подвержены развитию железодефицитной анемии дети, рожденные с большой массой, недоношенные, с лимфатико-гипопластическим диатезом.
Постнатальные железодефицитные анемии у детей связаны с факторами, действующими после рождения ребенка, прежде всего — недостаточным поступлением железа с пищей. В группе риска по развитию железодефицитной анемии находятся дети, получающие искусственное вскармливание неадаптированными молочными смесями, козьим или коровьим молоком. К алиментарным причинам железодефицитной анемии у детей также относятся поздние сроки введения прикормов, отсутствие в рационе животного белка, несбалансированное и нерациональное питание ребенка в любом возрасте.
К железодефицитной анемии у детей могут приводить наружные и внутренние кровотечения (желудочно-кишечные, в брюшную полость, легочные, носовые, травматические), обильные менструации у девушек и т. Дефицит железа сопутствует заболеваниям, протекающим с нарушением всасывания микроэлементов в кишечнике: болезни Крона, язвенному колиту, болезни Гиршпрунга, энтеритам, дисбактериозу кишечника, муковисцидозу, лактазной недостаточности, целиакии, кишечным инфекциям, лямблиозу и др.
Избыточная потеря железа отмечается у детей, страдающих кожными аллергическими проявлениями, частыми инфекциями. Кроме этого, причиной железодефицитной анемии у детей может выступать нарушение транспорта железа вследствие снижения содержания и недостаточной активности трансферрина в организме.
Симптомы железодефицитной анемии
Сидеропенический синдром связан с недостатком железа в тканях и проявляется нарушениями со стороны кожи и слизистых оболочек:
- сухость, дряблость, шелушение и трещины на коже;
- ломкость и слоистость ногтей, их поперечная исчерченность, койлонихия (ногти становятся плоскими, иногда принимают вогнутую «ложкообразную» форму);
- ангулярный стоматит (изъязвления и трещины в уголках рта);
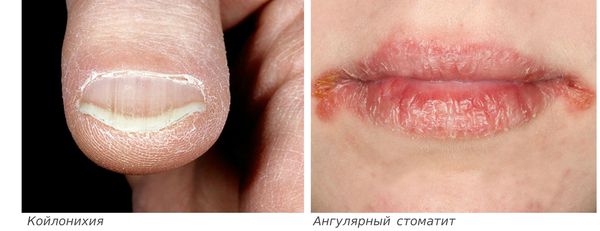
- ломкость и выпадение волос (волосы теряют блеск, истончаются, секутся, редеют и рано седеют);
- извращение вкуса и пристрастие к непищевым продуктам — к мелу, извести, глине, углю, краскам, земле и т. д.; причина этого симптома неизвестна, но он часто встречается при ЖДА;
- изменение обоняния и тяга к токсическим веществами — к бензину, керосину, мазуту, ацетону, лакам, краскам, гуталину, выхлопным газам, т. е. токсикомания; данный симптом необъясним, но тоже достаточно специфичен для ЖДА и полностью проходит на фоне приёма препаратов железа;
- недостаточность мышечных сфинктеров (недержание мочи при кашле, смехе, непреодолимые позывы к мочеиспусканию, возможно ночное недержание мочи).
Анемический синдром проявляется слабостью, быстрой утомляемостью, сонливостью днём и плохим засыпанием ночью, головокружениями, обмороками, частыми головными болями, шумом в ушах, мельканием «мушек» перед глазами, одышкой при физической нагрузке, увеличением частоты сердечных сокращений, неприятными ощущениями в области сердца, пониженным артериальным давлением.
При ЖДА может наблюдаться умеренное повышение температуры тела (до 37,5 °С), которое исчезает после лечения железосодержащими препаратами.
Зачастую снижение содержания гемоглобина происходит постепенно, при этом многие органы адаптируются к анемии. В связи с этим жалобы больных не всегда соответствуют показателям содержания гемоглобина. Многие пациенты, особенно женщины, свыкаются с неважным самочувствием, приписывая его переутомлению, психическим и физическим перегрузкам.
Патогенез железодефицитной анемии
Железо — жизненно важный для человека микроэлемент, который входит в состав гемоглобина крови, миоглобина мышц, отвечает за транспорт кислорода в организме и протекание многих биохимических реакций.
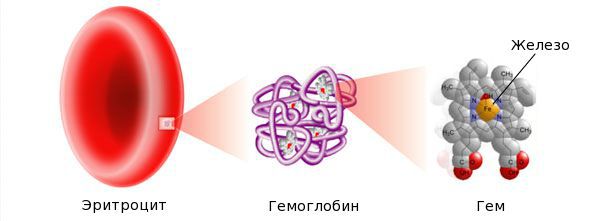
Железо поступает в организм в виде двухвалентного (мясная пища) и трёхвалентного (растительная пища) ионов. Первый всасывается легко, второй под действием соляной кислоты в желудке должен превратиться в двухвалентный. Далее он поступает в двенадцатиперстную кишку и начальные отделы тощей кишки, затем двухвалентное железо вновь переводится в трёхвалентное. В дальнейшем часть этого железа поступает в депо слизистой оболочки тонкой кишки, а другая всасывается в кровь, где соединяется с трансферрином (белком-переносчиком железа, синтезируемым в печени). Если содержание железа в организме избыточно, то оно задерживается в клетках кишечника и в дальнейшем удаляется из организма вместе со слущивающимся эпителием.
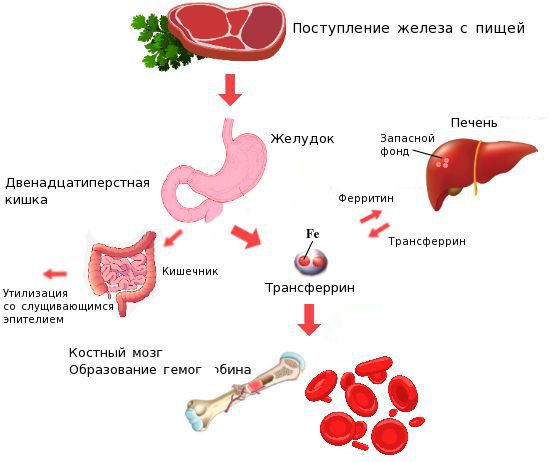
При снижении кислотности в желудке (атрофический гастрит, резекция желудка, приём препаратов, снижающих кислотность, гиповитаминоз С) нарушается ионизация железа в желудке, что ведёт к дальнейшему нарушению всасывания железа и развитию ЖДА. При резекции и хронических заболеваниях кишечника (дуоденит, хронический энтерит, целиакия) нарушается всасывание железа, что опять же приводит к развитию ЖДА.
Ферменты, содержащие железо, принимают участие в синтезе гормонов щитовидной железы и поддержании иммунитета, поэтому при дефиците железа нарушаются защитные и адаптационные силы организма и весь обмен веществ.
Классификация и стадии развития железодефицитной анемии
Выделяют три стадии железодефицитных состояний: прелатентный дефицит железа, латентный дефицит и железодефицитную анемию (ЖДА).
Для прелатентного дефицита железа характерно снижение запасов железа в костном мозге:
- снижение железа в депо (снижение ферритина);
- нормальный уровень сывороточного железа;
- нормальный уровень гемоглобина и эритроцитов;
На этой стадии симптомов может не быть.
Латентный (скрытый) дефицит железа влияет на тканевой обмен. На этой стадии запасы железа начинают истощаться, но организм ещё не успел отреагировать снижением гемоглобина. Возникают первые проявления заболевания — человека может беспокоить повышенная утомляемость, слабость, одышка при физической нагрузке, ломкость ногтей, сухость кожи, выпадение волос. Но эти симптомы пока выражены незначительно.
Латентный дефицит железа характеризуется:
- снижением железа в депо (снижение ферритина);
- снижением уровня сывороточного железа;
- нормальным уровнем гемоглобина и эритроцитов;
- повышением общей железосвязывающей способности сыворотки (ОЖСС);
- отсутствием гемосидерина (пигмента, состоящего из оксида железа, он образуется при распаде гемоглобина) в макрофагах костного мозга;
На третьей стадии (собственно ЖДА) снижается уровень гемоглобина и эритроцитов.
Для железодефицитной анемии характерно:
- снижение железа в депо (снижение ферритина);
- снижение уровня сывороточного железа;
- снижение уровня гемоглобина и эритроцитов;
- повышение общей железосвязывающей способности сыворотки (ОЖСС);
- отсутствие гемосидерина в макрофагах костного мозга;
- наличие тканевых проявлений (сидеропенический синдром);
- повышение растворимых трансферриновых рецепторов (рТФР);
- снижение коэффициента насыщения трансферрина железом (НТЖ);
- анизоцитоз — изменение размеров эритроцитов;
Для этой стадии характерна ярко выраженная клиническая симптоматика, хотя зачастую люди списывают эти проявления на переутомление.
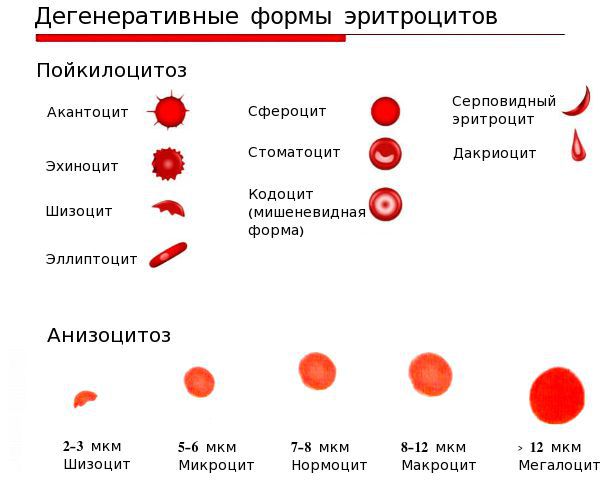
В норме уровень гемоглобина в крови: у женщин — 120-140 г/л, у мужчин — 130-160 г/л.
Степени тяжести ЖДА (на основании снижения уровня гемоглобина Hb):
- I — лёгкая степень: Hb от 90 до 120 г/л;
- II — средняя степень: Hb от 70 до 89 г/л;
- III — тяжёлая степень: Hb менее 70 г/л.
Осложнения железодефицитной анемии
Осложнения возникают при анемии, нелеченной более 5 лет. Тяжёлая ЖДА может привести к развитию миокардиодистрофии — поражению мышечного слоя сердца, снижению его сократительной функции и развитию сердечной недостаточности.
У беременных с ЖДА повышается риск преждевременных родов и задержки роста плода. У детей недостаток железа приводит к задержке роста и интеллектуального развития.
Редким и тяжёлым осложнением ЖДА является гипоксическая кома. Ей предшествует резкое побледнение кожных покровов и видимых слизистых, судороги, а затем потеря сознания. Гипоксия из-за недостатка железа осложняет течение уже имеющихся сердечно-лёгочных заболеваний, таких как ишемическая болезнь сердца, бронхиальная астма, хроническая ишемия головного мозга и способствует развитию неотложных состояний — острому или повторному инфаркту миокарда и острому нарушению мозгового кровообращения (инсульту).
Диагностика железодефицитной анемии
Минимальный объём исследований:
- клинический анализ крови с лейкоцитарной формулой;
- биохимический анализ крови (ферритин, сывороточное железо, общая железосвязывающая способность сыворотки, коэффициент насыщения трансферрина железом, растворимые трансферриновые рецепторы).
Биохимический анализ крови покажет снижение уровня сывороточного железа и ферритина, увеличение общей железосвязывающей способности сыворотки и растворимых трансферриновых рецепторов, снижение коэффициента насыщения трансферрина железом (НТЖ).
Лечение железодефицитной анемии
Лечение проводится железосодержащими препаратами, в основном для приёма внутрь и значительно реже для внутримышечного или внутривенного введения. Препараты нельзя принимать без назначения врача, так как переизбыток железа опасен своими последствиями — поражением зубов, развитием гепатита, цирроза печени, сахарного диабета и сердечно-сосудистых заболеваний. Также возможны тяжёлые аллергические реакции.
При анемии следует изменить рацион питания и включить в него продукты, содержащие железо в наиболее усвояемой форме — телятину, говядину, баранину, мясо кролика, печень, язык. Важно помнить, что из мяса усваивается до 30 % железа, из рыбы — 10 %, а из растительной пищи — всего лишь 3-5 %.
При анемии коррекция дефицита железа не может быть достигнута только изменением питания. Причина этого в том, что усвоение железа из пищи ограничено, а в препаратах оно содержится в большей концентрации.

При анемии лёгкой и средней степени тяжести препараты железа лучше принимать внутрь вместе с аскорбиновой или фолиевой кислотой, так как они улучшают всасываемость железа.
Если препараты железа невозможно применять внутрь (например, при непереносимости или нарушении всасывания железа в кишечнике), то их вводят внутримышечно или внутривенно. Инъекционные препараты железа используют только в стационаре, так как они могут вызывать шоковые реакции. Их нельзя применять во время беременности и лактации.
При тяжёлой анемии (гемоглобин менее 70 г/л) и по жизненным показаниям в условиях стационара проводят переливание эритроцитарной массы.
В качестве лечебно-профилактического средства пациентам, у которых нет сахарного диабета, можно использовать гематоген. В его состав входят железо, связывающее белки, получаемые из крови крупного рогатого скота, а также аскорбиновая кислота и необходимый комплекс белков. Однако это достаточно калорийный продукт — в 100 г гематогена содержится 350–500 килокалорий, об этом следует помнить, включая его в рацион.
Прогноз. Профилактика
Прогноз при ЖДА благоприятный. В большинстве случаев заболевание успешно лечится амбулаторно. Но если не анемию не лечить, то она может прогрессировать, ухудшая общее самочувствие. ЖДА сложно скорректировать в следующих случаях:
- при сопутствующих проблемах с ЖКТ (обострение хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки, воспалительных заболеваниях кишечника, синдроме мальабсорбции — нарушенного всасывания в кишечнике, резекции желудка и/или кишечника);
- одновременном приёме препаратов, снижающих всасывание железа;
- хронических кровопотерях;
- нелеченных системных и онкологических заболеваниях;
- нерегулярном приёме препаратов железа, несоблюдении дозировки, кратности и продолжительности приёма препарата или самостоятельной его замене.
Для профилактики ЖДА следует:
- ежегодно сдавать клинический анализ крови и контролировать его параметры;
- полноценно питаться, получая с пищей достаточное количество белка и железа;
- своевременно устранять источники кровопотери в организме;
- лицам из групп риска (донорам, детям, из спортивных школ, беременным и кормящим, а также женщинам, страдающим обильными и длительными менструациями) принимать небольшие дозы препаратов железа.
Железодефицитная анемия у детей

Железодефицитная анемия у детей – клинико-лабораторный синдром, развивающийся при дефиците железа в организме вследствие дисбаланса процессов его поступления, усвоения и расходования. Железодефицитная анемия у детей проявляется астено-вегетативным, эпителиальным, иммунодефицитным, сердечно-сосудистым и др. синдромами. Основными лабораторными критериями диагностики железодефицитной анемии у детей служат концентрация Hb, цветовой показатель, морфология эритроцитов, содержание железа и ферритина в сыворотке крови. Лечение железодефицитной анемии у детей включает соблюдение диеты и режима, прием препаратов железа, редко — переливание эритроцитарной массы.
В диагностике железодефицитной анемии и ее причин у детей участвуют различные специалисты: неонатолог, педиатр, гематолог, детский гастроэнтеролог, детский гинеколог и др. При осмотре ребенка обращает внимание наличие бледности кожных покровов и видимых слизистых (полости рта, конъюнктивы), акроцианоза или периорального цианоза, темных кругов под глазами.
Важнейшими лабораторными критериями, позволяющими судить о наличии и степени железодефицитной анемии у детей служат: Hb (<110 г/л), ЦП (<0,86), железо сыворотки крови (<14 мкмоль/л), общая железосвязывающая способность сыворотки (>63), ферритин сыворотки (<12 мкг/л) и др.
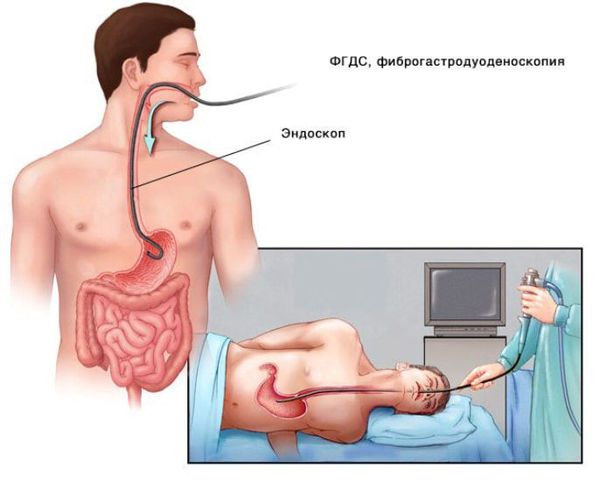
Для установления факторов и причин, сопутствующих железодефицитной анемии у детей, может потребоваться проведение пункции костного мозга; ФГДС, колоноскопии; УЗИ органов брюшной полости, УЗИ органов малого таза; рентгенографии желудка, ирригоскопии, исследования кала на дисбактериоз, скрытую кровь, яйца гельминтов и простейшие.
Лечение железодефицитной анемии у детей
К основным принципам лечения железодефицитной анемии у детей относятся: устранение причин железодефицита, коррекция режима и диеты, назначение препаратов железа.
Рацион детей, страдающих железодефицитной анемией, должен быть обогащен за счет продуктов, богатых железом: печени, телятины, говядины, рыбы, яичного желтка, бобовых, гречки, овсяных хлопьев, шпината, персиков, яблок и др.
Устранение дефицита железа в организме ребенка достигается благодаря приему железосодержащих препаратов. Детям младшего возраста препараты железа удобно назначать в виде жидких лекарственных форм (капель, сиропов, суспензий). Препараты железа следует принимать за 1-2 ч до еды, запивать водой или соками. В комплексную терапию железодефицитной анемии у детей необходимо включать витаминно-минеральные комплексы, адаптогены, фитосборы.
При железодефицитной анемии тяжелой степени детям проводится парентеральное введение препаратов железа, переливание эритроцитарной массы.
Основной курс лечения железодефицитной анемии у детей обычно составляет 4-6 недель, поддерживающий — еще 2-3 месяца. Одновременно с устранением железодефицита необходимо проводить лечение основного заболевания.
Прогноз и профилактика
Адекватное лечение и ликвидация причин железодефицитной анемии у детей приводит к нормализации показателей периферических крови и полному выздоровлению ребенка. У детей с хроническим дефицитом железа отмечается отставание в физическом и умственном развитии, частая инфекционная и соматическая заболеваемость.
Антенатальная профилактика железодефицитной анемии у детей заключается в приеме беременной ферропрепаратов или поливитаминов, предупреждении и лечении патологии беременности, рациональном питании и режиме будущей мамы. Постнатальная профилактика железодефицитной анемии у детей предусматривает грудное вскармливание, своевременное введение необходимых прикормов, организацию правильного ухода и режима ребенка. Профилактический прием препаратов железа показан недоношенным, близнецам, детям с аномалиями конституции, детям в периоды быстрого роста, полового созревания, девочкам-подросткам с обильными менструациями.
Патогенез В12-дефицитной анемии
Витамин B12 поступает в организм с продуктами животного происхождения: мясные продукты, яйца, сыр, молоко. Из связи с белками пищи витамин высвобождается сначала под воздействием кулинарной обработки, а затем соляной кислоты и ферментов желудочного сока.
В двенадцатиперстной кишке витамин B12 соединяется с внутренним фактором Кастла, который синтезируется париетальными клетками желудка. Благодаря фактору Кастла витамин B12 поступает в клетки слизистой оболочки подвздошной кишки. После этого он связывается с транспортным белком транскобаламином II и переносится кровью клеткам-потребителям, в основном в печень и костный мозг.
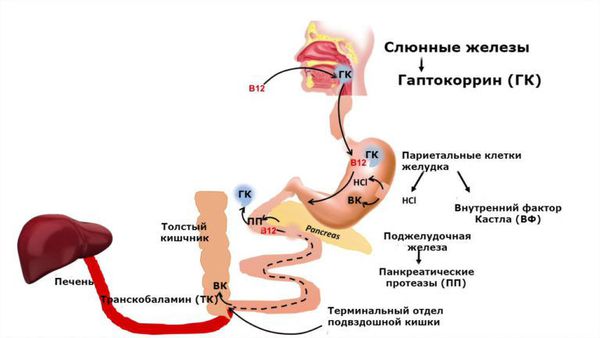
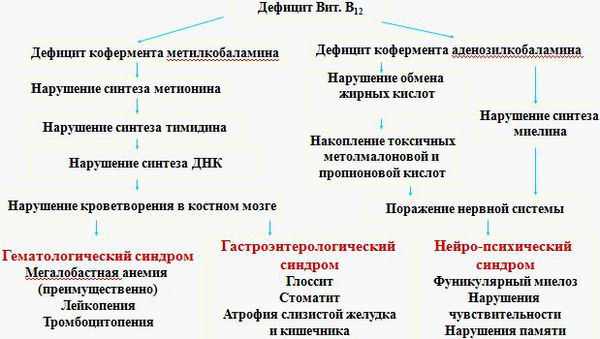
В клетке витамин B12 преобразуется в два кофермента: метилкобаламин и аденозилкобаламин. Коферменты — это соединения, необходимые для функционирования ферментов.
Метилкобаламин является коферментом для фермента метионинсинтазы, который преобразует одну аминокислоту — гомоцистеин в другую — метионин. При сбое этого процесса в организме накапливается гомоцистеин, не образуются пиримидиновые основания, необходимые для формирования ДНК. В результате нарушается синтез ДНК и процессы деления клеток. К этому изменению особенно чувствительны быстроделящиеся клетки — кроветворные клетки костного мозга, из которых образуются клетки крови, а также эпителиальные клетки желудочно-кишечного тракта. Отсюда появление таких изменений в анализе крови, как анемия, лейкопения (снижение количества лейкоцитов), тромбоцитопения (снижение количества тромбоцитов), а также атрофия слизистых оболочек.
Классификация и стадии развития В12-дефицитной анемии
Классификация В12ДА по причинам развития:
- Наследственные (врождённые) формы. Описаны у детей с генетическими аномалиями, которые приводят к нарушению транспорта и метаболизма витамина B12.
- Приобретённые формы:
Стадии развития B12ДА:
- Начальная — латентный дефицит. Уровень витамина в сыворотке крови снижен, однако число эритроцитов и уровень гемоглобина остаются в норме. Клинических проявлений на данной стадии может не наблюдаться. Лабораторно возможно выявить изменение параметров эритроцитов: увеличение среднего объёма эритроцита (параметр MCV в анализе крови) и среднего содержания гемоглобина в эритроците (параметр MCH).
- Стадия клинических проявлений. Наблюдается при снижении уровня гемоглобина, когда появляются симптомы анемии, и при поражении нервной системы.
Степени тяжести В12ДА:
- Лёгкая — снижение уровня гемоглобина до 90 г/л.
- Средней тяжести — уровень гемоглобина в пределах 90-70 г/л.
- Тяжёлая — уровень гемоглобина ниже 70 г/л.
Осложнения В12-дефицитной анемии
Задержка роста и развития у детей возможна в результате снижения гемоглобина при B12ДА.
Потеря массы тела может стать результатом снижения аппетита и проявлений со стороны желудочно-кишечного тракта.
Присоединение инфекционных осложнений возможно при развитии глубокой лейкопении (низкого уровня лейкоцитов). Снижение тромбоцитов, как правило, незначительное и не приводит к геморрагическим осложнениям.
Также описано такое тяжёлое осложнение B12ДА, так тромботическая микроангиопатия — заболевание, в основе которого лежит поражение мелких сосудов и формирование в их просвете тромбов, что сопровождается воспалением сосудистой стенки. Как следствие, может развиваться ишемия органов и тканей.
Диагностика В12-дефицитной анемии
Для правильной постановки диагноза B12ДА важен осмотр врача-гематолога. Для уточнения и коррекции проблем, связанных с работой желудочно-кишечного тракта, потребуется консультация гастроэнтеролога. Для оценки неврологических проявлений может быть необходим осмотр врача-невролога.
При осмотре врач может обратить внимание на бледность и лёгкую желтушность кожи, увеличение частоты сердечных сокращений и расширение границ сердца. Необходимо провести осмотр полости рта, особенно языка. Невролог может оценить тонус мышц и наличие патологических рефлексов.
Одним из самых важных этапов диагностики является оценка клинического анализа крови. В анализе наблюдается:
- снижение гемоглобина — анемия;
- макроцитоз — наличие в крови большого количества аномально крупных эритроцитов (макроцитов);
- гиперхромия — интенсивное окрашивание эритроцитов, вызванное повышенным количеством гемоглобина в крови;
- может наблюдаться снижение числа лейкоцитов и тромбоцитов.
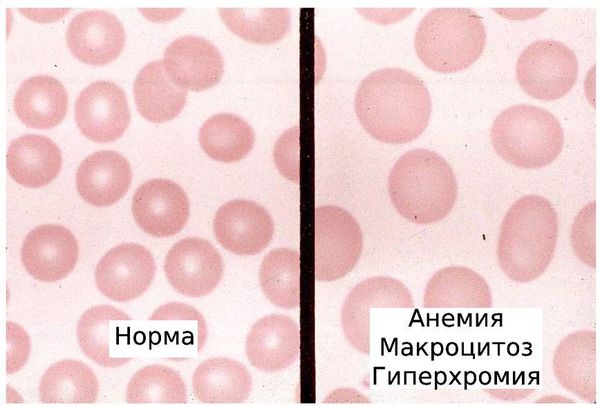
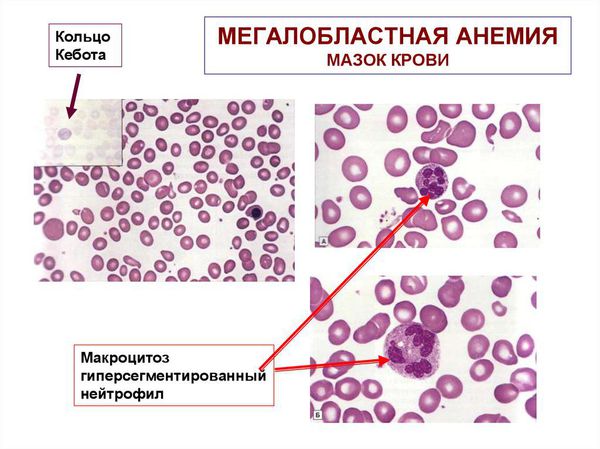
Необходимо выполнение мазка крови, в котором врач-морфолог может увидеть патологические формы эритроцитов:
- овалоциты (эритроциты овальной формы) и дегенеративные формы;
- увеличение разницы эритроцитов по своему размеру (параметр RDW);
- специфические патологические включения, такие как тельца Жолли и кольца Кебота;
- мегалоциты и мегалобласты — в тяжёлых случаях.
Могут встречаться также патологические формы нейтрофилов:
- гигантские нейтрофилы;
- нейтрофилы с гиперсегментацией ядра (5 и более сегментов);
- метамиелоциты — незрелые нейтрофильные лейкоциты.
В биохимическом анализе крови:
- снижен уровень витамина B12;
- уровень железа и ферритина в норме.
В общем анализе мочи может наблюдаться стойкая протеинурия — появление белка в моче. В ряде случаев отмечается повышение уровня метилмалоновой кислоты и гомоцистеина.
Дополнительные лабораторные исследования, которые могут помочь выявить причину дефицита витамина B12:
- исследование антител к внутреннему фактору Кастла (IgG) и париетальным клеткам желудка в сыворотке крови;
- исследование желудочного сока на выявление внутреннего фактора Кастла и антител к этому фактору (IgA, синтезируются париетальными клетками желудка);
- тест Шиллинга — определяет активность внутреннего фактора Кастла и всасывание витамина B12 в кишечнике;
Возможна пренатальная диагностика генетически обусловленной недостаточности транспортного белка транскобаламина II, поскольку он синтезируется амниоцитами (клетками плодной оболочки).
При ультразвуковом исследовании органов брюшной полости можно обнаружить незначительную гепатоспленомегалию — увеличение печени и селезёнки.
Дифференциальный диагноз при В12-дефицитной анемии, особенно со снижением лейкоцитов и тромбоцитов, проводится с такими заболеваниями системы крови:
- Миелодиспластический синдром — группа гематологических заболеваний, при которых костный мозг не производит достаточного количества одного или более типов клеток крови: тромбоцитов, лейкоцитов, эритроцитов.
- Апластическая анемия — это анемия, возникающая вследствие недостаточной продукции эритроцитов из-за уменьшения количества кроветворных стволовых клеток.
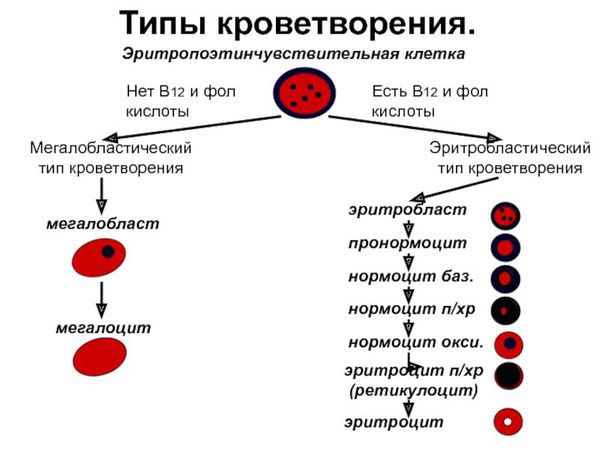
Для уточнения диагноза может потребоваться выполнение пункции костного мозга и его морфологическое исследование. При наличии B12ДА специалист морфолог описывает в костном мозге характерные изменения стволовых клеток-предшественников:
- гиперплазию (разрастание) эритроидного ростка — стволовых клеток-предшественников, из которых образуются эритроциты;
- мегалобластный тип кроветворения, при котором образуются крупные клетки с зернистыми ядрами, патологические митозы, тельца Жолли;
Лечение В12-дефицитной анемии
При анемии, которая связана с недостаточностью поступления витамина с пищей, лечение предполагает коррекцию диеты в комбинации с внутримышечным введением витамина B12. Диета с достаточным содержанием витамина B12 предполагает употребление продуктов животного происхождения. Овощи, фрукты, хлеб не содержат витамин B12.

При других причинах коррекция диеты будет неэффективна. Во всех случаях лечение подразумевает введение препарата витамина В12 по стандартным схемам. Дозы препарата могут отличаться в зависимости от возраста больного и от наличия неврологических симптомов.
Лечение обычно проводится в амбулаторных условиях. Показанием для госпитализации в стационар может послужить тяжёлая анемия (уровень гемоглобина менее 70 г/л) и пожилой возраст.
При подозрении на B12ДА без лабораторного её подтверждения категорически не рекомендуется начинать лечение витамином B12 либо поливитаминными комплексами, поскольку введение B12 приводит к быстрому исчезновению морфологических аномалий клеток, что в свою очередь затруднит постановку правильного диагноза. Ошибочное использование фолиевой кислоты при дефиците B12 может привести к усугублению неврологических симптомов. Поэтому очень важно начинать терапию только после лабораторного подтверждения диагноза.
Первый этап терапии — насыщение. Он длится 4-6 недель и предполагает внутримышечное введение препарата цианокобаламин в лечебной дозе. В некоторых случаях может быть эффективно использование сублингвальных форм витамина B12. Признаки улучшения состояния наблюдаются после первых 3-5 инъекций препарата.
Первым лабораторным признаком эффективности терапии является ретикулярный криз — повышение уровня ретикулоцитов в крови в 2-3 раза по сравнению с исходным на 4-7 день от начала терапии. Нормализация уровня гемоглобина достигается через 1-2 месяца, периферическая нейропатия купируется медленнее.
На фоне терапии цианокобаламином в связи с активным делением клеток-предшественников в костном мозге возможно присоединение дефицита фолиевой кислоты и железа, поэтому спустя 7-10 дней от начала терапии витамином B12 необходимо дополнительно назначить фолиевую кислоту, а при снижении уровня ферритина — препараты железа.
Второй этап — закрепляющая терапия: витамин B12 вводится в той же дозе, но кратность введения уменьшается.
Независимо от возраста больного, при ранней постановке диагноза, своевременном начале лечения и правильном наблюдении после выздоровления прогноз при B12ДА благоприятный. Ухудшению прогноза могут способствовать сопутствующие сердечно-сосудистые заболевания у пожилых больных, а также поражение нервной системы (фуникулярный миелоз).
Анемия у детей (Малокровие)
Анемия у детей — это гематологический синдром, характеризующийся снижением концентрации гемоглобина и количества эритроцитов в единице объема крови. При различных формах анемии у детей отмечаются общая слабость, быстрая утомляемость, бледность кожи и слизистых, головокружение, сердцебиение. Анемия у детей диагностируется по клиническим и лабораторным данным (общий анализ крови, определение билирубина, сывороточного железа, общей железосвязывающей способности сыворотки, исследование пунктата костного мозга и т. Общие принципы лечения анемии у детей включают организацию рационального питания, своевременное введение прикормов, витаминотерапию, прием препаратов железа, ФТЛ (гимнастика, массаж, УФО), по показаниям — проведение гемотрансфузий.
Частое возникновение анемии у детей обусловлено их интенсивным ростом, активностью процесса эритропоэза, прогрессивным увеличением числа форменных элементов и ОЦК. Вместе с тем, аппарат кроветворения у детей функционально незрел и весьма уязвим перед лицом различных воздействий. Нормальное протекание кроветворения у детей требует большого количества железа, белка, витаминов и микроэлементов, поэтому любые погрешности вскармливания, инфекции, токсические воздействия на костный мозг способны вызвать развитие анемии у ребенка. Особенно чувствительными в этом плане оказываются дети второго полугодия жизни, у которых истощены неонатальные резервы железа.
Длительно существующая анемия у детей сопровождается развитием гипоксии, глубокими тканевыми и органными изменениями. Дети с анемией отстают в физическом и умственном развитии от здоровых сверстников, чаще страдают интеркуррентными заболеваниями, склонны к развитию хронических патологических процессов и различного рода осложнений.
В соответствии с этиопатогенезом выделяют следующие группы анемий:
Постгеморрагические анемии у детей, обусловленные с острой или хронической кровопотерей.
Анемии у детей, обусловленные нарушением гемопоэза:
- железодифицитные (гипохромные)
- наследственные и приобретенные железонасыщенные (сидероахрестические — связаны с дефектами синтеза порфиринов)
- мегалобластные (В12–дефицитные и фолиеводефицитные)
- наследственные и приобретенные дизэритропоэтические
- наследственные и приобретенные гипопластические и апластические (связаны с угнетением кроветворения)
III. Наследственные и приобретенные гемолитические анемии у детей, обусловленные повышенным разрушением эритроцитов и преобладанием процесса кроворазрушения над процессом кровообразования (мембранопатии, ферментопатии, гемоглобинопатии, аутоиммунные анемии, гемолитическая болезнь новорожденных и др.
Основу диагностики анемии у детей составляют лабораторные исследования. В общем анализе крови при анемии у детей выявляется снижение гемоглобина (Hb менее 120-110 г/л), снижение Er (<3,8х1012/л), снижение ЦП <0,85. Биохимическое исследование крови включает определение сывороточного железа, насыщения трансферрина железом, концентрации ферритина в сыворотке, билирубина, витаминов. В некоторых случаях требуется проведение пункции и исследования костного мозга.
В процессе диагностики определяется форма и степень тяжести анемии у детей. Последняя оценивается по содержанию эритроцитов и гемоглобина:
- анемия легкой степени – Hb 110-90 г/л, Er — до 3,5х1012/л;
- анемия средней степени — Hb 90-70 г/л, Er — до 2,5х1012/л;
- анемия тяжелой степени — Hb менее 70г/л, Er — менее 2,5х1012/л.
По показаниям дети с анемией могут нуждаться в консультациях узких специалистов (детского гастроэнтеролога, детского ревматолога, детского нефролога, детского гинеколога и др. ), обследовании ЖКТ (ЭГДС, УЗИ брюшной полости) и почек (УЗИ почек).
Лечение анемии у детей
При анемии у детей требуется организация правильного режима дня и сбалансированного питания ребенка, проведение лекарственной терапии и общеукрепляющих мероприятий. Детям рекомендуется достаточное пребывание на свежем воздухе, дополнительный сон; назначается гимнастика и массаж, УФО.
Детям с анемией, находящимся на грудном вскармливании, следует своевременно вводить прикормы (соки, яичный желток, овощи, мясное пюре). Одновременно необходимо скорректировать рацион кормящей женщины, добавить прием поливитаминов и препаратов железа. Детям, получающим искусственное вскармливание, назначаются адаптированные молочные смеси, обогащенные железом. Диета детей старшего возраста должна содержать печень, говядину, бобовые, зелень, морепродукты, фруктовые и овощные соки.
Медикаментозная терапия анемии у детей включает назначение препаратов железа и поливитаминных препаратов до полной нормализации клинико-лабораторных показателей (в среднем 6-10 недель). В тяжелых случаях может потребоваться проведение гемотрансфузии.
Прогноз железодефицитных анемий у детей обычно благоприятный. При своевременной диагностике, правильной организации питания, лечении анемии и сопутствующих заболеваний наступает полное выздоровление. Тяжелая анемия у детей может явиться основанием для переноса сроков вакцинации.
Антенатальный этап профилактики анемии у детей включает полноценное питание беременной, достаточное пребывание на свежем воздухе, прием минерально-витаминных комплексов, содержащих железо. Постнатальное предупреждение анемии у детей сводится к естественному вскармливанию, введению прикормов в рекомендуемые сроки, профилактике заболеваний раннего возраста, организации хорошего ухода и оптимального режима для ребенка, проведению превентивных лечебно-профилактических курсов в группах риска.
Литература1. Анемии новорожденных: диагностика профилактика, лечение. -Клинические рекомендации. — 2015. Классификация и диагностика анемий у детей/ Румянцев А. // Вопросы современной педиатрии. — 2011. — Т. 10, №1. Гемолитические анемии у детей/ А. Моргун, Т. Таранушенко. — 2018. Код МКБ-10D64
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
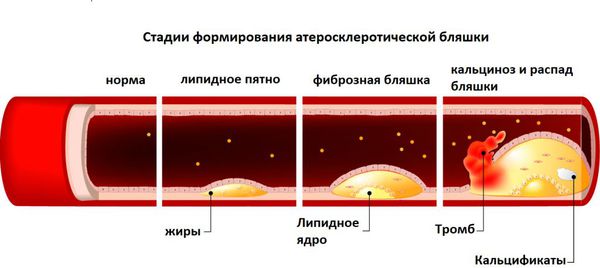
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям — гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний — сидеробластной анемии, талассемии.

К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др. ; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.

В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
